截至2019年底 医疗器械标准制修订任务已完成89.4%

医药网7月13日讯 7月8日,国家药监局发布《中国医疗器械标准管理年报(2019)》显示,截至2019年底,“十三五”规划中500项医疗器械标准制修订任务已立项447项,已完成89.4%。
上述年报显示,2019年共发布国家标准5项、行业标准72项以及行业标准修改单3项,医疗器械标准共计1671项,医疗器械标准技术体系持续优化。
截至2019年底,现行有效医疗器械标准中有基础标准273项、管理标准54项、方法标准406项、产品标准938项。
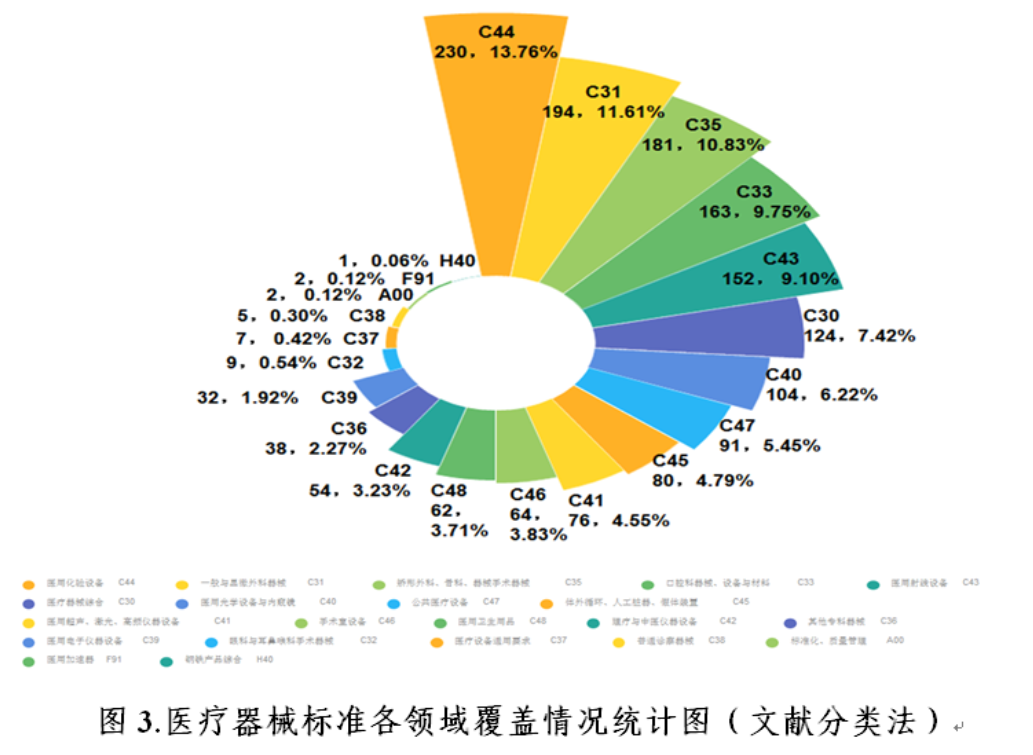
按照《中国标准文献分类法》,医疗器械标准主要归类在C30至C49之间,C10和C30代表医药和医疗器械综合,其他代号指代的领域多为具体的产品领域。
从现有医疗器械标准领域分布情况看,占比前5位的分别是:医用化验设备(C44)13.8%,一般与显微外科器械(C31)11.6%,矫形外科、骨科器械(C35)10.8%,口腔科器械、设备与材料(C33)9.8%,医用射线设备(C43)9.1%。
按照标委会(技术归口单位)归口领域,标准数量排名前5位的分别是:医用电气设备领域339项(20.3%),体外诊断领域243项(14.5%),外科植入物领域209项(12.5%),口腔材料和器械163项(9.8%)和输液器具领域148项(8.9%)。
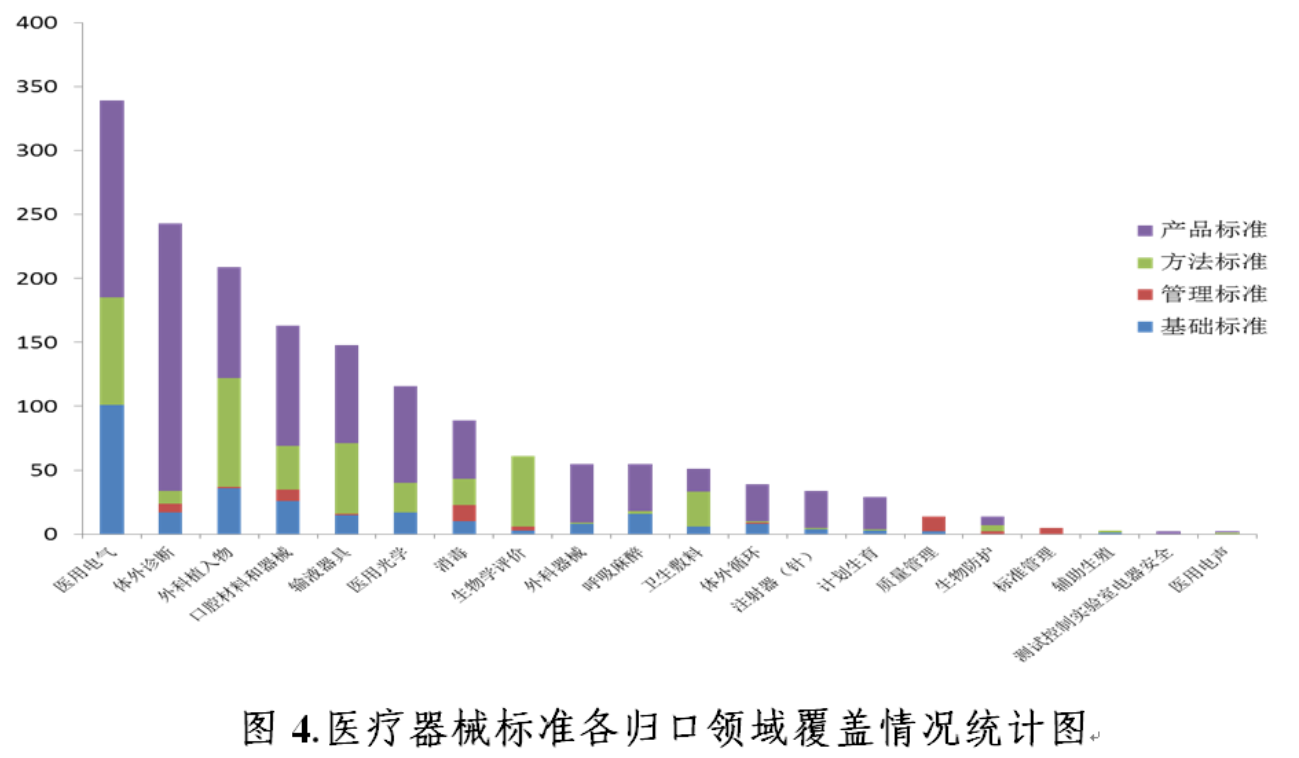
在各归口领域中,根据不同领域的标准需求,标准类别有所不同,医用电气设备、呼吸麻醉领域的基础标准占比较高,均达29.0%。
医疗器械标准管理和质量管理领域的管理标准占比最高,分别为100%和85.7%。
医疗器械生物学评价领域的方法标准占比最高,达90.2%。
计划生育和体外诊断医疗器械领域的产品标准占比最高,分别为86.2%和86.0%。
医疗器械标准的技术支撑
上述年报显示,标委会(技术归口单位)是医疗器械标准制修订的承担主体,也是医疗器械标准体系组织架构的重要组成部分。
从1980年第一个医疗器械标准化技术委员会成立以来,经过40年的发展,标委会(技术归口单位)数量已逐步增长到32个(13个总技委、13个分技委和6个技术归口单位。
医疗器械标准工作领域不断拓展,医疗器械标准组织架构进一步完善,有利于充分发挥新形势下医疗器械标准的引领作用和技术支撑作用。
此外,相关部门还及时加大标准信息公开力度,提高标准可及性,在国家药品监督管理局医疗器械标准管理中心网站公开医疗器械标准文本,实现医疗器械行业标准目录和强制性医疗器械行业标准文本100%对外公开。
2019年,对外公开第一批636项非采标推荐性医疗器械行业标准文本,非采标推荐性行业标准文本对外公开率达87%。
同时不断加强标准制修订信息公开,提高标准参与度,通过信息化手段继续扩大标准制修订过程信息的对外公开,保证标准制修订工作的透明、公开,提高各方参与度。
具体包括扩大标准立项项目来源、广泛征求标准意见、探索标准反馈机制等。
转载:医药网

